Костномозговая трансплантация как метод лечения лейкоза
Одним из методов лечения лейкоза является костномозговая трансплантация, которая может быть эффективна при продвинутых стадиях заболевания. Трансплантация проводится путем пересадки костного мозга от донора пациенту.
Костный мозг содержит стволовые клетки, которые могут развиваться в кровяные клетки, необходимые для выработки крови и борьбы с инфекциями. Пересадка костного мозга восстанавливает работу и продукцию здоровых кровяных клеток в организме пациента.
Трансплантация костного мозга может быть аллогенной, когда донором выступает другой человек, или аутологичной, когда донором является сам пациент, у которого заблокирована и сохранена часть его собственных стволовых клеток. Аутологичная трансплантация более безопасна, но результаты аллогенной трансплантации могут быть более эффективными при тяжелых случаях лейкоза.
Костномозговая трансплантация может иметь побочные эффекты, такие как риск инфекций, кровотечений, ослабления иммунной системы. Определение возможности проведения трансплантации зависит от некоторых факторов: стадии, типа и прогресса заболевания, возраста и общего состояния здоровья пациента.
В целом, костномозговая трансплантация может помочь пациентам с лейкозом, которые не отвечают на другие методы лечения. Однако, ее применение всегда рассматривается индивидуально как показательно для конкретного случая.
1.Что такое лейкемия, типы лейкоза
Лейкемия, или лейкоз – это рак крови. Лейкемия начинается в костном мозге – мягких тканях внутри костей. Именно в костном мозге вырабатываются клетки крови.
У здоровых людей костный мозг состоит из разных типов клеток:
- Белых кровяных клеток, которые помогают организму бороться с инфекцией;
- Красных кровяных телец, которые переносят кислород во все части Вашего тела;
- Тромбоцитов, которые отвечают за свертываемость крови.
У людей с лейкозом костный мозг начинает производить большое количество белых кровяных клеток, называемых лейкозными. При этом лейкозные клетки не выполняют функции нормальных белых кровяных клеток, растут быстрее, чем обычные клетки, и их рост не прекращается тогда, когда в норме это должно произойти.
Со временем лейкозные клетки вытесняют здоровые клетки крови, в том числе эритроциты и тромбоциты. Это может привести к серьезным проблемам, таким как анемия, кровотечения и инфекции. Лейкозные клетки также могут распространиться на лимфатические узлы и другие органы и вызвать их опухание и боль.
Какие бывают типы лейкоза?
Есть несколько видов лейкемии. В целом лейкоз классифицируется в зависимости от того, насколько быстро ухудшается болезнь и на какие белые кровяные клетки лейкоз влияет.
- Лейкоз может быть острым или хроническим. Острый лейкоз прогрессирует очень быстро и приводит к ухудшению самочувствия сразу же. Хроническая лейкемия прогрессирует медленно, и может не вызывать никаких симптомов лейкоза в течение многих лет;
- Лейкемия может быть лимфоцитарной лейкемией или лейкозом. Лимфоцитарный, или лимфобластный лейкоз влияет на белые кровяные клетки, называемые лимфоцитами. Миелолейкоз поражает белые кровяные клетки, которые называются миелоцитами;
Исходя из этих критериев выделяют четыре основных типа лейкемии:
- Острый лимфобластный лейкоз;
- Острый миелобластный лейкоз, или сотрый миелолейкоз;
- Хронический лимфоцитарный лейкоз;
- Хронический миелолейкоз.
У взрослых наиболее распространенными типами лейкоза является хронический лимфолейкоз и острый миелобластный лейкоз. Лейкоз у детей чаще всего проявляется в форме острого лимфобластного лейкоза. Встречается у детей и острый миелобластный лейкоз и другие виды миелоидой лейкемии, такие как хронический миелолейкоз и миеломоноцитарный лейкоз.
Существуют и менее распространеннее типы лейкоза, такие как волосатый клеточный лейкоз, и подтипы лейкемии, например – промиелоцитарная лейкемия.
Что представляет собой заболевание
Острый лейкоз — болезнь кровеносной системы, провоцирующая сбой в функционировании клеток костного мозга. У здорового человека белые клетки крови (лейкоциты и лимфоциты) способствуют уничтожению мутировавших злокачественных клеток. Вследствие попадания вирусов/инфекций, наследственных факторов, ионизирующего облучения, воздействия опасных канцерогенов, курения, употребления алкоголя и других причин (истинные причины развития белокровия не изучены) происходит сбой в работе лейкоцитов и лимфоцитов, приводящий к нарушению их пролиферации. В результате стволовая клетка, подвергшаяся мутации, перестает вырабатывать здоровые клетки, воспроизводя особую группу лейкозных клонов с измененными признаками. Они, в свою очередь, начинают производить клетки-мутанты, часть из которых — опухолевые бласты — бесконтрольно размножаются сначала на определенном участке костного мозга, в последующем расселяясь по всему организму, поражая кожные покровы, почки, печень, головной мозг.
Острой форме лейкемии свойственно избыточное образование бластов с последующим заражением крови. От того, клетки какого ростка — миелопоэзного/лимфопоэзного — мутируют, различают два вида острой лейкемии:
- острый лимфобластный лейкоз (ОЛЛ) — сопровождается беспорядочным, бесконтрольным размножением лимфобластов, по статистике в 80% случаев фиксируется у детей, поражая обычно оболочки спинного и головного мозга;
- острый миелоидный лейкоз (ОМЛ) — распространенная форма белокровия у взрослых, приводящая к неуправляемому размножению лейкозных клеток в костном мозге и к подавлению других кровяных ростков.
Избыточная концентрация лейкоцитов и лимфоцитов приводит к:
- повышению густоты крови;
- увеличению размеров печени и поджелудочной железы (гепатоспленомегалии);
- ухудшению зрения, вплоть до потери;
- проявлению болевого синдрома за грудиной, в пояснице, в подложечной области;
- изменению периферического кровообращения.
Вероятность летального исхода при остром течении болезни велика. Острой форме лейкоза не свойственно перерождение в хроническую. Консервативное лечение, как правило, неэффективно при резком увеличении количества бластных клеток.
При остром лейкозе прогноз жизни определяется следующими факторами:
- форма недуга;
- стадия развития болезни;
- возраст больного.
Согласно статистике у людей среднего возраста, вероятность победить злокачественный недуг, добившись состояния стойкой ремиссии, выше, чем у пожилых людей. У последних прогноз чаще неблагоприятный из-за сниженного уровня природного иммунитета. В то время как маленькие пациенты быстрее и легче справляются с лейкозом.
Лечение
Ребенка, страдающего лейкозом, в обязательном порядке госпитализируют, так как лечение возможно только в условиях стационара. Терапия направлена на достижение следующих результатов:
- Уничтожение патологических клеток.
- Поддержка и укрепление иммунной системы.
- Предотвращение присоединения инфекционных заболеваний.
- Нормализация состава крови (увеличение количества эритроцитов и тромбоцитов).
Существует несколько разновидностей терапевтических методов для лечения лейкоза.
Наиболее действенными среди них считается химиотерапия, лучевая терапия, пересадка костного мозга.
Выбор того или иного метода зависит от нескольких факторов, таких как:
- стадия развития заболевания;
- разновидность патологических клеток и их содержание;
- факторы риска возникновения рецидивов.

Лечение осуществляется поэтапно:
- На подготовительном этапе осуществляются непродолжительные курсы химиотерапии, при этом ребенку назначают и препараты, нормализующие деятельность почек, задачей которых является выведение из организма продуктов распада патологических клеток;
- Индуктивный этап длительностью 5-8 недель, предполагает более продолжительные курсы химиотерапии с использованием сразу нескольких различных препаратов. Цель данного этапа — достижение улучшения состояния ребенка;
- Комплексный этап. Наряду с химиотерапией ребенку назначают процедуру облучения. В некоторых случаях в спинномозговой канал вводят препараты цитостатической группы;
- Повторный индуктивный этап — представляет собой курсы химиотерапии с использованием сильнодействующих препаратов. Длительность курса и этапа определяется врачом индивидуально;
- Этап поддержания. На данном этапе лечения ребенку вводят небольшие дозы активного вещества. Лечение осуществляется амбулаторно. Ребенок в этот период уже может посещать общественные образовательные учреждения.
Рекомендации по лечению диффузного токсического зоба у детей вы найдете на нашем сайте.
Клиническая картина
Симптомы лейкоза у детей складываются из проявлений нескольких синдромов – комплексов патологических изменений.
Первые признаки лейкемии обычно неспецифичны: субфебрильная (в районе 37 градусов) температура, слабость, быстрая утомляемость, потливость. Так проявляется интоксикационный синдром.
- Гиперпластический синдром: это такие признаки лейкоза у детей как увеличенные лимфоузлы, селезенка, печень. Это связано с тем, что лейкозные клетки накапливаются в этих органах. Возможно и «метастазирование» — формирование лейкемических бляшек на коже, слизистых. С частотой 5 – 20% развивается нейролейкоз – лейкозные инфильтраты формируются в головном мозге. И если увеличение лимфоузлов, печени и селезенки, как правило, безболезненно и бессимптомно, за исключением случаев, когда они сдавливают жизненно важные органы, то нейролейкоз обычно проявляется признаками менингита или повышенного внутричерепного давления – тошнотой, рвотой, нарушением сознания.
- Анемический синдром. Симптомы лейкемии у детей, связанные с анемией возникают из-за того, что стремительное размножение лейкозных клеток не оставляет места для нормального кроветворения. Малыш становится бледным, неактивным, при малейшей физической нагрузке возникает одышка. Примерно в трети случаев гемоглобин падает до 60 г/л и ниже (при минимальной норме для трехлетнего возраста 110 г/л).
- Геморрагический синдром. Эти симптомы рака крови у детей связаны с кровотечениями. Бесконтрольное размножение лейкозных клеток угнетает размножение эритроцитов, но и тромбоцитов – кровяных клеток, отвечающих за свертывание крови. Проявляется частыми и бесконтрольными кровотечениями: в виде мелких точечных кровоизлияний, обильных носовых или желудочных кровотечений. Возможно и излитие крови в полость мозга – то, что случается при геморрагических инсультах.
- Синдром инфекционных осложнений. Этот признак лейкемии у детей возникают из-за резкого снижения иммунитета. Лимфоциты – это клетки крови, которые отвечают за распознавание инфекционного агента и выработку антител к нему. Незрелые формы, которые преобладают при детской лейкемии, неспособны выполнять свою работу. Если лейкемия возникла у ребенка, инфекции развиваются в 80 – 85%. Это пневмонии, различные гнойные процессы, вплоть до сепсиса (заражения крови). В последние годы в случаях лейкозов у детей встречаются и вирусные инфекции – герпес, цитомегаловирус.
Профилактика Острого лимфобластарного лейкоза:
Профилактика
Дозу 24 Гр на голову дают на 3 недели по 1,5 Гр за сеанс с двух латеральных полей.
Одну из двух инъекций метотрексата, вводимого 2 раза в неделю в спинномозговой канал, во время облучения головы целесообразно производить в субботу, так как в этот день, как правило, не бывает лучевой терапии, другую – в один из первых дней недели
после сеанса облучения головы; в день эндолюмбального введения метотрексата больной остается в стационаре.
В период профилактики нейролейкемии с помощью как облучения, так и введения метотрексата и цитозара, больные получают внутрь 6-меркаптопурин ежедневно в дозе 25 мг/м2 и циклофосфамид в дозе 100 мг/м2 1 раз в неделю.
После окончания профилактики нейролейкемии делают пункцию костного мозга, и если признаков рецидива нет, то начинают поддерживающую терапию.
Вторым методом профилактики нейролейкемии является эндолюмбальное введение метотрексата и цитозара. Препараты вводят с интервалом 3-4 дня, при плохой переносимости 1 раз в неделю.
Оба метода профилактики нейролейкемии надежны и позволяют отказаться от поддерживающих интралюмбальных введений метотрексата.
Непрерывное поддерживающее лечение в период улучшения острых лимфобластного и недифференцируемого лейкозов детей проводится амбулаторно, в течение 5 лет до полного улучшения. Начинают лечение сразу после достижения полного улучшения или после курсов, закрепляющих достигнутое улучшение.
Дети получают непрерывное лечение тремя препаратами по следующей схеме: 6-меркаптопурин внутрь ежедневно; метотрексат внутрь на 6-й день недели; циклофосфамид внутрь на 7-й день недели, в эти дни 6-меркаптопурин не отменяют.
Для «группы риска» в период непрерывного поддерживающего лечения тремя препаратами каждые 1,5-2 месяца проводится курс СО АР. Во время данного курса в течение недели после него поддерживающее лечение тремя препаратами отменяется, а затем в течение недели проводится половинными дозами. После этого поддерживающее лечение проводится полными дозами.
Условия проведения непрерывного лечения:
1) анализ крови с определением тромбоцитов и ретикулоцитов 1 раз в неделю;
2) при снижении уровня лейкоцитов до 1 Ч 103 – 2 Ч 103 (1000-2000) в 1 мкл врач снижает дозу цитостатических препаратов вдвое, при последующем его повышении более 2,5 Ч 103 (2500) в 1 мкл восстанавливают прежнюю дозу;
3) лечение прерывают на любом этапе при падении уровня лейкоцитов в крови ниже 1000 в 1 мкл, при значительном повышении температуры, стоматите, диарее;
4) пункцию костного мозга в первый год улучшения производят 1 раз в месяц; на 2-5-м году улучшения – 1 раз в 3 месяца.
Лечение острого лимфобластного лейкоза усиливается, когда речь идет о процессе Т-клеточной природы. По программе американских педиатров-онкологов для устранения проявлений болезни при Т-лимфобластном остром лейкозе начинают с внутривенного введения циклофосфана по 1200 мг/м2 в 1-й день лечения или между 2-м и 5-м днем (при уровне лейкоцитов более 5 Ч 104 (50 000) в 1 мкл и значительной органомегалии, требующих предварительного назначения аллопуринола из-за высокого уровня мочевой кислоты в сыворотке и опасности развития мочекислого диатеза). С 3-4-го дня (или в 1-й день, если введение циклофосфана отсрочено) еженедельно (1 раз в неделю) по этой программе, как и по программе Aur, вводится винкристин в течение 4 недели, а также
применяют преднизолон и рубомицин в дозах и в сроки, соответствующие схеме 2 лечения острого лимфобластного лейкоза.
При достижении ремиссии проводится курс ее консолидации, включающий 5-дневное непрерывное введение цитозара по 100 мг/(м2/сут.), прием тиогуанина (или 6-меркаптопурина) по 50 мг/м2 каждые 12 ч в течение 5 дней введения цитозара. Проводят 3 курса лечения цитозаром и тиогуанином (6-меркаптопурин) с интервалом между курсами 14 дней.
Затем в течение 7-14 дней внутривенно капельно вводят L-acnapaгиназу по 200-300 ЕД/кг. В случае высокого уровня лейкоцитов и большой массы опухолевых лимфатических узлов спленомегалии или гепатомегалии терапию нужно проводить, назначая больному большое количество жидкости, щелочное питье, наряду с аллопуринолом для профилактики мочекислого диатеза.
Если при Т-клеточном остром лейкозе в средостении определяются увеличенные лимфатические узлы, плохо сокращающиеся от химиотерапии, то рекомендуется локальное облучение этой области в дозе 30 Гр; локальное облучение целесообразно и при значительном увеличении лимфатических узлов любой другой области.
Лечение в период улучшения при Т-клеточном лейкозе должно быть усилено: наряду с непрерывной терапией 6-меркаптопурином, метотрексатом, циклофосфаном.
Диагностика Лейкоза у детей:
Механизм развития
В основе становления патологического процесса лежит группа особенностей, факторов. Можно выделить такие моменты:
Генетическая мутация во внутриутробном периоде
Если верить специальным исследованиям, острый лимфобластный лейкоз (ОЛЛ) начинается с формирования клетки-клона. То есть такой цитологической единицы, которая отличается от нормальной и весьма существенно. Не может выполнять свои функции, зато очень быстро делится.
При этом какое-то время организм держит ситуацию под собственным контролем. Как только происходит толчок — начинается развитие патологического процесса.
Таким триггером может стать все что угодно: от перенесенной инфекции и до воспалительного аутоиммунного расстройства. Затем клетка начинает активно делиться. Как и ее потомки. Процесс развивается в геометрической прогрессии.
Клон, согласно все тем же исследованиям, закладывается еще в период внутриутробного развития. Насколько быстро это приведет к патологическому состоянию — сказать заранее трудно. Почти невозможно.
Влияние радиации
Ионизирующее излучение оказывает критическое воздействие на клетки костного мозга. Даже в самых малых дозировках. Развивается типичный патологический процесс.
Наступают мутации. Что в конечном итоге и приводит к началу расстройства. Причиной лимфобластного лейкоза в острой форме становится выработка неполноценных клеток, которые не способны выполнять свои функции. К тому же — обладают высокой пролиферативной активностью.
В некоторых случаях патология становится настолько стойкой, что справиться с ней не удается.
Воздействие инфекционного фактора
Сравнительно редкая причина. Вирусы действительно способны вызвать генетические мутации. Но это скорее исключение из правил.
В основной же части случаев речь идет об инфекции как о триггере патологического процесса. То есть клетка, которая потенциально способна делиться, аномальная цитологическая структура ужу существует. А вирус/бактерия кладут непосредственное начало расстройству.
Если вовремя взять источник инфекции под контроль, есть шансы не столкнуться с острым лимфобластным лейкозом.
Прочие генетические аномалии
Обычно комплексного характера. Часто патологический процесс встречается у пациентов, которые страдают мутациями. Например, при синдроме Дауна и прочих состояниях.
С чем это связано — точно не известно. По всей видимости, механизм развития патологического процесса примерно одинаковый.
Острый лимфобластный лейкоз манифестирует, преимущественно, у детей. То есть развивается в первые годы жизни.
Если говорить точнее, особая опасность — это диапазон от 5 до 12-13 лет. Затем вероятность падает вполовину. Но и у взрослых пациентов развитие патологического процесса все еще возможно.
Диагностика
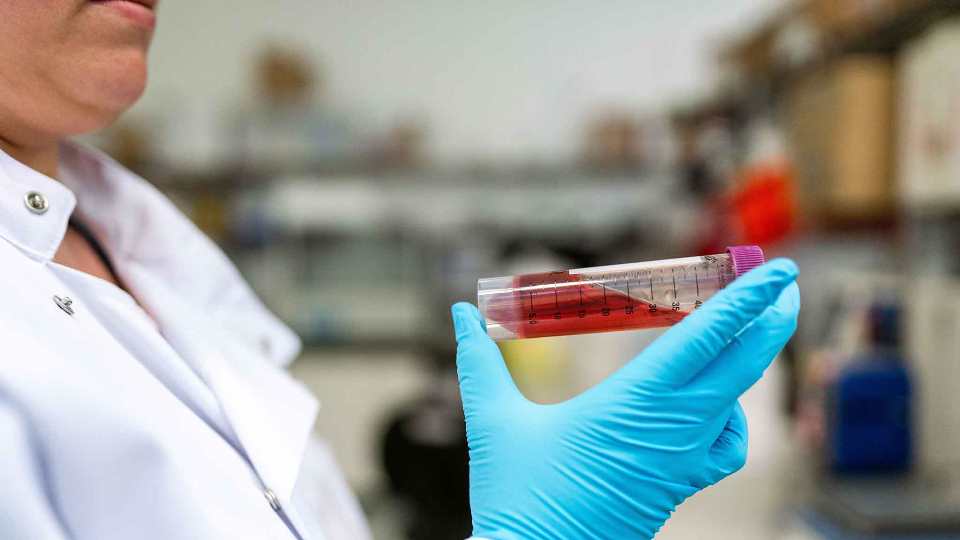
Основными процедурами в диагностике лейкоза являются лабораторные анализы крови: общий, биохимический, генетический.
Не менее важны исследования пункции костного мозга и цереброспинальной жидкости:
- цитогенетическое, выявляющее атипичные хромосомы, характерные для изменённых клеток;
- цитохимическое, позволяющее выявить на ранней стадии острую форму заболевания;
- иммунофенотипическое, в результате которого становится понятно, какие типы клеток подверглись злокачественному изменению;
- миелограмма, позволяющая определить стадию заболевания и динамику процесса.
Одновременно пациенту назначают инструментальные исследования внутренних органов — УЗИ, КТ, МРТ, чтобы определить лейкозную инфильтрацию.
Симптомы
Первые признаки заболевания развиваются с увеличением в составе крови незрелых лимфоцитов:
- бледность кожи;
- быстрая утомляемость;
- повышенная температура тела;
- чрезмерное выделение пота, особенно по ночам;
- частые простуды;
- кровоподтёки и синяки на коже;
- потеря веса без видимых причин.
По мере распространения лейкозных клеток развиваются симптомы острого лимфоцитарного лейкоза, свидетельствующие о поражении других органов:
- головные боли, нарушения зрения и слуха, ухудшение координации движений, онемение лицевых мышц при проникновении в головной мозг и нервную систему;
- боли в костях и суставах при тотальном поражении костного мозга;
- боли в правом подреберье при метастазировании в печень и селезёнку.
Могут встречаться и другие проявления болезни, в зависимости от локализации повреждений.
Симптомы лейкоза у детей

Для клинической картины болезни характерно общее ухудшение самочувствия, постоянна слабость, боль в мышцах, снижение активности и повышение температуры тела. Выявить болезнь на ранних стадиях, без проведения лабораторных тестов, невозможно, потому что ее признаки имеют схожесть с простым ОРВИ.
Не всегда болезнь имеет легкое начало, в отдельных случаях клиника проявления схожа с картиной острого сепсиса. Температура тела повышается до критических отметок, развивается ангина и диатез, осложняется дыхание, на коже возникают петехии и экхимозы, проявляется внутреннее кровотечение.
Поскольку лейкоциты отвечают за защиту организма, заподозрить лейкемию можно по увеличению частоты заболеваемости гриппом и ОРВИ. Эти болезни при раке крови сложно поддаются лечению и часто протекают с осложнениями.
Первые признаки
Первые признаки лейкоза у заболевающих, проявляются так:
- сильная утомляемость организма;
- снижение аппетита;
- нарушения сна;
- незначительное, но беспричинное повышение температуры тела;
- быль в мышцах, костях и суставах.
Внимание!
Ранние симптомы лейкемии у детей схожи с проявлениями обычной простуды, потому родители вряд ли смогут идентифицировать болезнь самостоятельно и своевременно, поэтому посещать врача нужно регулярно, не пренебрегая необходимостью сдачи крови на анализ.
У детей симптомы также включают увеличение размеров печени и селезенки, по телу образуются красные пятна. Болезнь может сопровождаться симптомами интоксикации организма, тошнотой, рвотой, диареей и носовыми кровотечениями.
При остром течение

Острый лейкоз у детей проявляется с разной интенсивностью. Эта особенность зависит от степени злокачественности процесса. Измененные клетки поражают организм и активно размножаются, потому клиническая картина отягощается.
Отмечается возникновение таких симптомов:
- снижение гемоглобина;
- анемия, вялость, повышенная утомляемость;
- геморрагический синдром, кровоизлияния;
- кровоточивость десен, кровь из носа, снижение свертываемости крови;
- выраженный иммунодефицит, повышенная восприимчивость к инфекционно-вирусным болезням;
- общая интоксикация: отказ от пищи, неукротимая рвота, лихорадка;
- сосудистые изменения, сбой сердечного ритма;
- желтушность слизистых, склер глаз, кожи;
- увеличение размеров и болезненность узлов лимфатической системы;
- головокружение, острые головные боли;
- парез конечностей.
Лейкоз у новорожденных приводит к отставанию в развитии. Грудной ребенок отказывается от еды, плохо набирает вес, питание обеспечивается искусственно, через капельницу.
Хроническая форма болезни
Хронический лейкоз у детей можно разделить на два вида:
- лимфобластный;
- миелобластный.
Каждое заболевание имеет свои симптомы и требует конкретного воздействия.
При лимфобластном раке крови возникают такие признаки:
- общее истощение организма;
- слабость;
- головокружение;
- гипергидроз;
- увеличение лимфатических узлов;
- увеличение селезенки и печени;
- учащенное сердцебиение;
- нарушение сна.
Внимание!
Хронический лейкоз, перенесенный в детском возрасте, имеет последствия для женской и мужской половой системы. У мужчин болезнь провоцирует импотенцию и бесплодие, а у женщин – аменорею.
При лимфобластном малокровии прослеживается значительное изменение лейкоцитарной формулы с увеличением массы лимфоцитов в крови до 95 %. Масса тромбоцитов изменяется незначительно или остается заниженной, существенно уменьшается гемоглобин. При хронической форме болезни, ее симптомы могут проявиться спустя 3-8 лет.
Миелобластное белокровие прогрессирует постепенно и провоцирует появление таких признаков:
- боль в скелете и мышцах;
- бледность кожи;
- кровотечение из носа и десен;
- гипергидроз;
- потеря веса;
- слабость.
При этом типе поражения увеличение лимфатических узлов не прослеживается. Болезнь развивается в течение 3-5 лет.
Симптомы Острого лимфобластного лейкоза:
Различают два типа течения острого лимфобластного лейкоза: В-линейный и Т-линейный, в зависимости от типа клеток – лимфоидных предшественников.
Все лейкоциты в организме человека делятся на 2 типа – гранулоцитарные и агранулоцитарные (зернистые и незернистые), эти две группы, в свою очередь, подразделяются на эозинофилы, базофилы, нейтрофилы (гранулоцитарные), и лимфоциты (В- и Т-типа) и моноциты (агранулоцитарные). В процессе созревания и развития (дифференцировки) все клетки проходят несколько этапов, первым из которых является бластный этап (лимфобласты). Из-за поражения костного мозга опухолью, лимфоциты не успевают достаточно развиться для того, чтобы полноценно исполнять свои защитные функции. По большей части, при остром лимфобластном лейкозе поражаются В-лимфоциты (примерно в 85% случаев), отвечающие за образование антител в организме.
Клинические признаки острого лимфобластного лейкоза
- Синдром интоксикации – слабость, лихорадка, недомогание, потеря веса. Лихорадка может быть связана и с наличием бактериальной, вирусной, грибковой или протозойной (реже) инфекцией, особенно у детей с нейтропенией (менее 1500 нейтрофилов в 1 мкл).
- Гиперпластический синдром – увеличение всех групп периферических лимфоузлов. Инфильтрация печени и селезенки приводит к их увеличению, что может проявляться болями в животе. Могут появиться боль и ломота в костях из-за лейкемической инфильтрации надкостницы и суставной капсулы и опухолевого увеличения объема костного мозга. При этом на рентгенограммах можно обнаружить характерные для лейкемической инфильтрации изменения, особенно в трубчатых костях, возле крупных суставов.
- Анемический синдром – бледность, слабость, тахикардия, кровоточивость слизистых полости рта, геморрагический синдром на коже, бледность. Слабость возникает в результате анемии и интоксикации.
- Геморрагический синдром связан как с тромбоцитопенией, так и с внутрисосудистым тромбозом (особенно при гиперлейкоцитозе) и приводит к появлению петехий, экхимозов на коже и слизистых, кровоизлияниям, мелене, рвоте с кровью.
- У мальчиков может обнаруживаться инициальное увеличение яичек ( 5-30% случаев первичного ОЛЛ). Это безболезненные, плотные, одно- или двусторонние инфильтраты. Особенно часто это бывает при гиперлейкоцитозе и Т-клеточном варианте ОЛЛ.
- Дыхательные нарушения, связанные с увеличение лимфоузлов средостения, которые могут привести к дыхательной недостаточности. Этот признак характерен для Т-линейного ОЛЛ.
- Могут появиться кровоизлияния в сетчатку глаза, отек зрительного нерва. При офтальмоскопии могут обнаруживаться лейкемические бляшки на глазном дне.
- Из-за сильно сниженного иммунитета любое повреждение кожи является очагом инфекции, могут появиться паронихии, панариции, инфицированные укусы насекомых и следы инъекций.
Достаточно редкими осложнениями могут являться поражения почек в результате инфильтрации (клинические проявления могут и отсутствовать) и выпотной перикардит из-за нарушения лимфооттока между эндокардом и эпикардом.
Диспансерное наблюдение
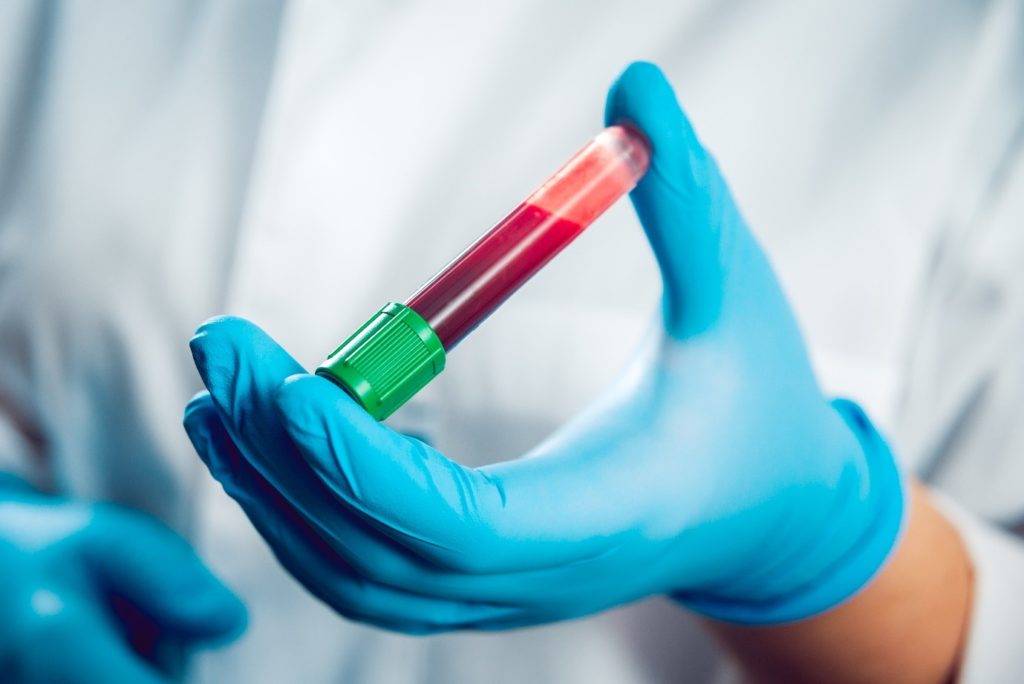
Рис.5 Исследование крови
В ремиссии детям и подросткам с заболеванием лейкозом требуется диспансерное наблюдение. Реабилитация должна быть комплексной. Кроме медицинской помощи необходимо учитывать социально-психологические аспекты восстановления ребенка, возращения его в нормальную жизнь. Здесь нужно участие социальных работников, психологов и педагогов. Программа реабилитации разрабатывается в индивидуальном порядке, исходя из степени сложности лечения, наличия психологических и социальных проблем.
В период диспансерного наблюдения за ребенком проводятся следующие исследования и осмотры специалистов:
- До завершения поддерживающего лечения один раз в неделю необходим общий анализ крови. После окончания терапии его делают раз в месяц.
- 1 раз в три месяца кровь берут на биохимический анализ. Когда поддерживающее лечение окончено, анализ берут раз в полгода.
- Таким же образом проводится УЗИ органов малого таза, брюшной полости, забрюшинного пространства, осмотр ребенка гематологом.
Если у пациента в процессе лечения возникла патология других органов, то периодичность осмотров смежными специалистами устанавливается индивидуально. С диспансерного учета ребенка снимают, когда окончена поддерживающая терапия, есть устойчивая ремиссия и отсутствуют сопутствующие заболевания. После завершения лечения должно пройти не менее пяти лет.





































