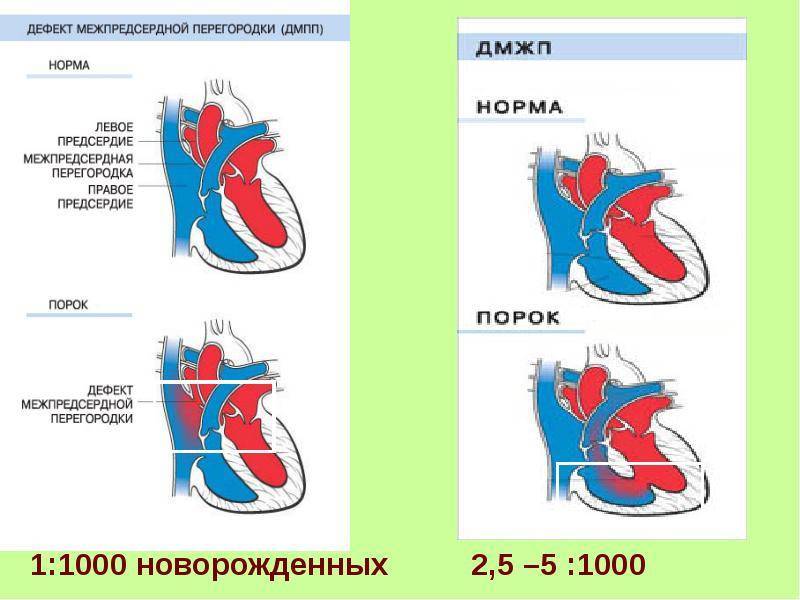
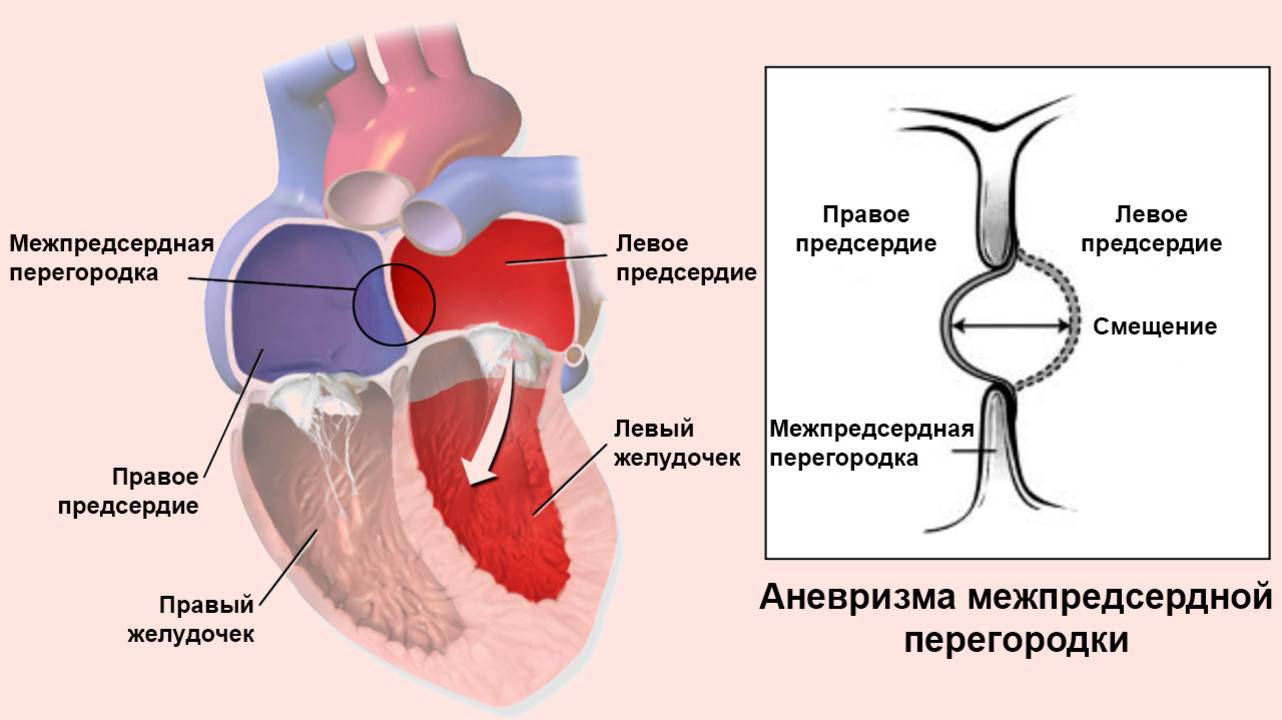
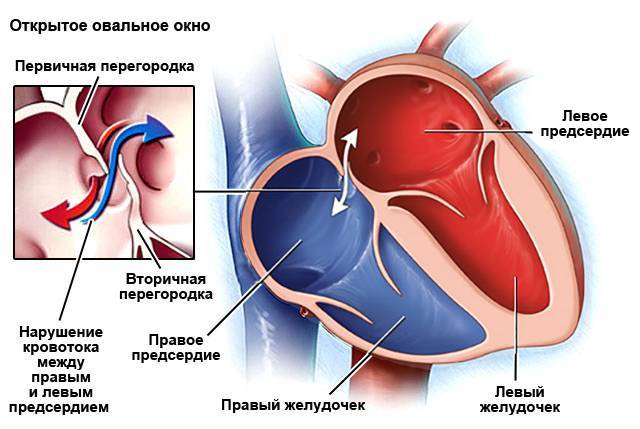
Патогенез или особенности гемодинамики
Внутриутробное развитие плода имеет много особенностей. Один из них — плацентарное кровообращение. Наличие РАС не нарушает сердечную функцию плода. После рождения отверстие закрывается само по себе, и кровь начинает циркулировать по легким. В противном случае кровь сливается слева направо, и правый желудочек становится гиперемированным и гипертрофированным.
При тяжелых РАС гемодинамика меняется на 3-й день после рождения. Легочные сосуды переполняются, правые желудочки перегружаются и гипертрофируются, повышается артериальное давление, увеличивается легочный кровоток, развивается легочная гипертензия. Застой в легких и инфекция приводят к развитию отека легких и пневмонии.
Затем начинается легочный вазоспазм и переходная фаза легочной гипертензии. Младенец поправляется, становится более активным и больше не болеет. Период стабилизации — лучшее время для радикальной операции. Если этого не сделать вовремя, легочные сосуды начинают необратимо склеротизировать.
Камеры сердца претерпевают компенсаторную гипертрофию, стенки артерий и артериол утолщаются, становятся плотными и неэластичными. Давление в желудочках постепенно выравнивается, и венозная кровь начинает течь из правого желудочка в левый. У новорожденного развивается тяжелое состояние, называемое артериальной гипоксемией, с характерными клиническими симптомами. В начале болезни вено-артериальный выпот временно появляется при физической нагрузке, кашле и упражнениях, а затем становится постоянным и сопровождается одышкой и цианозом в покое.
Симптомы и клинические проявления
Симптомы зависят от тяжести нарушения, индивидуальных обстоятельств и частично от возраста пациента. Если размер овального отверстия небольшой, симптомов нет. Больные не испытывают дискомфорта. Ребенок активен, нормально развивается, объективных отклонений в состоянии здоровья не имеет. Однако в любой момент патологический процесс может активизироваться и проявиться серьезными симптомами и осложнениями.
В других случаях клиническая картина присутствует, но не конкретна. Родители могут связывать аномалии с внутричерепным давлением, аллергией, дисбактериозом и другими процессами в раннем детстве.
- Одышка. Частота движений увеличивается. Однако это можно увидеть только путем целенаправленных измерений. Частота дыхания достигает 40 и более, что свидетельствует о нарушении нормального газообмена. Причина может заключаться не только в сердце, но и в легких. Требуется более подробное объяснение.
- Слабость. Ребенок вялый, сонный. Отдыхаю больше обычного. Это может быть особенностью организма в начальный период. Но самочувствие не меняется по мере взросления, что должно насторожить родителей. Возможные аномалии структур сердца.
- Непостоянство. Другой вариант. Это проявляется постоянным плачем без видимых на то причин. Это основание для консультации педиатра.
- Расстройства пищевого поведения. Ребенок не может есть. Ей нужны частые перерывы в кормлении, чтобы отдышаться. Это ненормально и указывает на нарушение подачи кислорода.
- Бледная кожа. По всему телу. Меняют оттенок и слизистые оболочки, что хорошо видно на деснах.
- Никакого быстрого набора веса. Истощение тканей, снижение скорости накопления жира и недостаточный метаболизм мышечных волокон.
- То же самое и с ростом. Ребенок отстает в физическом развитии по сравнению со сверстниками. По мере прогрессирования патологии это становится все более очевидным. Если лечение проводится, отклонения сглаживаются.
- Возможный застой в легких. Проявляется частыми пневмониями или бронхитами практически с первых дней жизни.
Поскольку в основе заболевания лежит недостаточная деятельность малой кровеносной системы, страдает дыхательная система. Отсюда характерные аномалии. Этот факт может стать отправной точкой для профессиональной оценки состояния здоровья маленького пациента. Не всегда кардиологические РАС у детей выявляются в первые недели и даже годы патологии. Около четверти людей диагностируется с этим дефектом в возрасте от 16 до 25 лет. В это время легче диагностировать анатомический дефект, страдающий человек может рассказать о своем самочувствии. Однако к этому моменту неисправность существует уже несколько десятилетий, поэтому оказывается, что ею можно пренебречь.
- Одышка. Визитная карточка незакрытого овального окна. Постоянно следует за пациентом, практически не уходит. Умеренный в покое, позволяет нормальный отдых. При небольших физических нагрузках он усиливается, приводит к генерализованным нарушениям гемодинамики, в том числе поражению головного мозга. Выполнение профессиональных обязанностей может быть трудным, как и домашние обязанности.
- Боль в сердце. Они имеют неясное происхождение, легкие и иногда невозможно связать с сердечными заболеваниями. Они недолговечны, длятся не более минуты, чаще даже короче. Это происходит не у половины всех людей.
- Бледная кожа. Во время. Пациент выглядит как восковая фигура. При нарушениях гемодинамики возникает постоянно.
- Повышенное потоотделение. Гипергидроз. Это не имеет ничего общего с упражнениями.
- Слабость, сонливость, утомляемость даже при малой активности и значительная потеря трудоспособности. Он также не может выполнять домашние дела. Астения вызвана недостаточным снабжением структур мозга кровью и питательными веществами.
- Те же причины могут вызвать головокружение, головокружение (неспособность ориентироваться) и тошноту. Рвота бывает редко.
- Удушье. Сильное нарушение газообмена. Это происходит не всегда. Усиливается в положении лежа на спине. Это может быть вызвано отеком легких или сердечной астмой.
- Обморок. Обморочные состояния вызваны внезапным снижением питания мозга. Отрицательная прогностическая точка. Это указывает на необходимость срочного хирургического лечения.
Симптомы неспецифические. Решение принимают врачи, которые принимают его после тщательного обследования здоровья человека.
Причины дефекта межпредсердной перегородки
Проблемы с зарастанием овального окна, прочие нарушения формирования перегородки сердца во внутриутробном периоде могут иметь следующие причины:
- патология носит наследственный характер;
- прием матерью в период вынашивания запрещенных веществ, злоупотребление алкоголем, курение;
- токсикозы, гестозы;
- терапия на начальных сроках антибиотиками, психотропными, гормонозамещающими и противоэпилептическими средствами;
- радиационное и ионизирующее воздействие;
- вредные и опасные условия труда матери;
- тяжелые инфекционные и вирусные заболевания, перенесенные матерью в первые месяцы (грипп, герпес, краснуха, ветрянка);
- нарушения эндокринной системы беременной.
Также причиной развития дефектов могут стать экологические факторы. Влияние на организм вредных веществ, находящихся в воздухе, часто приводит к различного рода мутациям.
Катетеризация сердца.
В настоящее время большинство вторичных ДМПП с подходящей морфологией могут быть закрыты с помощью чрескожного катетерного метода. Если эта процедура технически невыполнима или не подходит пациенту, то рекомендуется выполнение стандартного открытого хирургического вмешательства.
В этой процедуре врачи вставляют тонкую трубку (катетер) в кровеносный сосуд в паху и направляют его к сердцу, используя методы визуализации. Через катетер врачи устанавливают сетчатый пластырь или пробку, чтобы закрыть отверстие. Ткань сердца растет вокруг сетки, постоянно закрывая отверстие.
Что такое дефект межпредсердной перегородки и какие бывают формы заболевания?
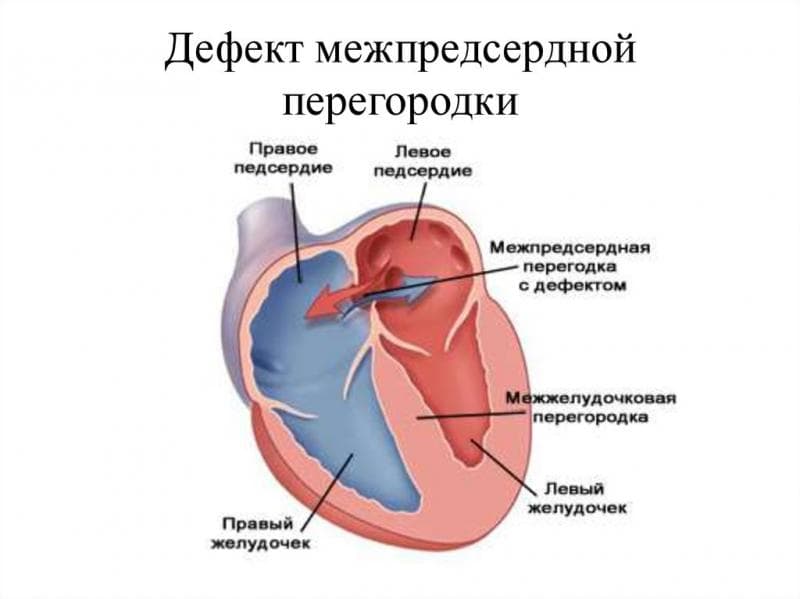
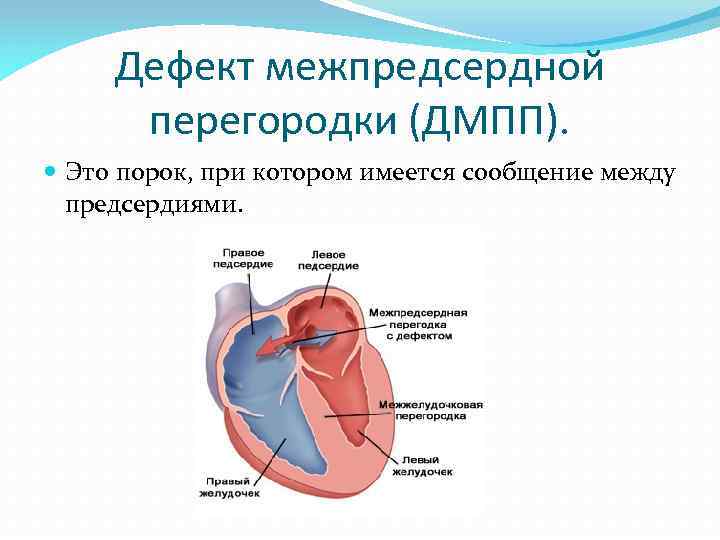
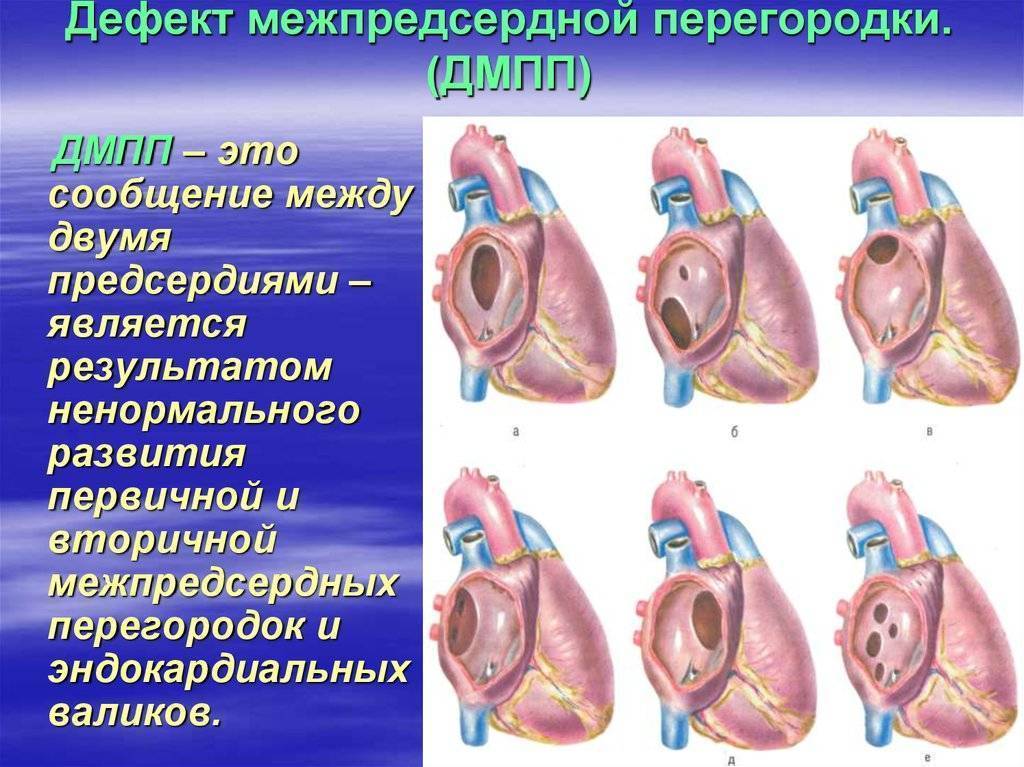
ДМПП – это врожденный порок сердца, при котором правое и левое предсердие сообщаются между собой. Выделяют три вида дефекта межпредсердной перегородки:
- Открытое овальное окно. Во время внутриутробного развития у эмбриона полностью отсутствует перегородка между предсердиями. Благодаря этому, в организме плода до момента раскрытия легких происходят процессы газообмена. Впоследствии окно закрывается особым клапаном, который должен плотно примыкать к перегородке, но иногда его размеры не совпадают с размерами отверстия. Иногда различные физические или психоэмоциональные нагрузки приводят к тому, что клапан отстает от перегородки и кровь из одного предсердия попадает в другое.
- Первичный дефект межпредсердной перегородки. Это состояние ребенка характеризуется дефектами клапанов, расположенных между предсердиями и желудочками. В межпредсердной перегородке остается просвет.
- Вторичный дефект межпредсердной перегородки. У новорожденного есть нарушение строения полой верхней вены.
Не всегда ДМПП диагностируется во время рождения. Зачастую болезнь протекает бессимптомно, только на УЗИ сердца у многих взрослых обнаруживается подобная патология. Врожденные пороки сердца встречаются достаточно часто. На 1 млн. новорожденных у 600 тыс. есть проблемы с сердцем, причем диагноз ДМПП более характерен для женского пола.
Лечение
Первичный и вторичный сердечные пороки при незначительной степени выраженности принято просто наблюдать. Нередко они могут самостоятельно зарастать, но позднее положенного срока. Если подтверждается прогрессирование дефекта в перегородке, то наиболее целесообразно хирургическое вмешательство.
Пациентам назначается и медикаментозное лечение. Основная цель такой терапии – устранить нежелательные симптомы и снизить риск развития вероятных осложнений.
Консервативная помощь
Перед назначением лекарственных препаратов учитываются все особенности пациента. При необходимости их меняют. Наиболее распространенными группами считаются следующие:
- диуретики;
- бета-блокаторы;
- сердечные гликозиды.
Из числа мочегонных препаратов назначается «Фуросемид» или «Гипотиазид». Выбор средства зависит от степени распространенности отеков
В процессе лечения важно соблюдать дозировку. Увеличение суточного количества мочи приведет к нарушению проводимости в сердечной мышце
Дополнительно к этому артериальное давление упадет, что закончится потерей сознания. Такое последствие связано с дефицитом калия и жидкости в организме.
«Анаприлин» чаще всего назначается в детском возрасте из группы бета-блокаторов. Его задача заключается в уменьшении потребностей в кислороде и частоты сокращений. «Дигоксин» (сердечный гликозид) повышает объем циркулирующей крови, расширяет просвет в сосудах.
Хирургическое вмешательство
При появлении дефекта между предсердиями, операция не относится к числу экстренных. Пациенту можно выполнять ее, начиная с возраста 5 лет жизни. Хирургическое лечение по восстановлению нормальной анатомии сердца бывает нескольких форм:
- открытая операция;
- закрытие дефекта через сосуды;
- ушивание вторичного дефекта в перегородке;
- пластика с помощью заплаты;
Основными противопоказаниями к оперативному вмешательству является тяжелое нарушение свертываемости крови, острые инфекционные заболевания. Стоимость указанных операций зависит от сложности процедуры, использования материала для закрытия отверстия между предсердиями.
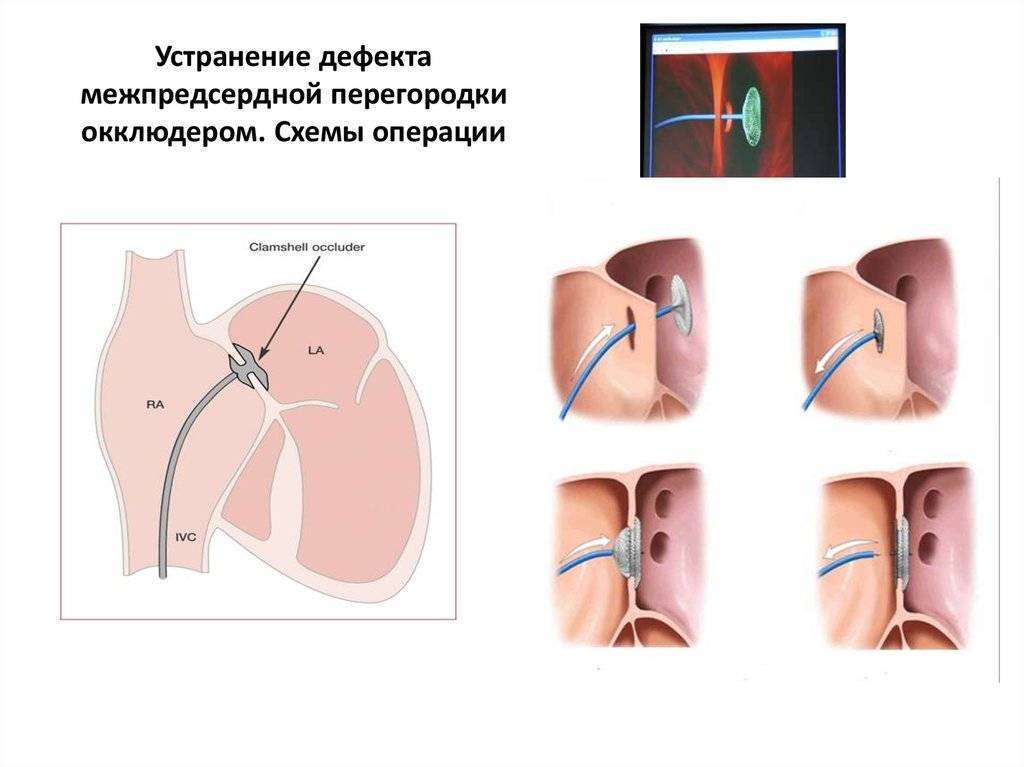
Эндоваскулярный (внутрисосудистый) метод закрытия ДМПП
Схема имплантацииокклюдера
Эндоваскулярный (внутрисосудистый) метод закрытия дефекта межпредсердной пререгородки (ДМПП) начал развиваться с 1975 года. Устройство для эндоваскулярного закрытия дефекта получило название окклюдер. В последующие годы было испытано несколько поколений окклюдеров, но только с 2001 года устройства получили международное одобрение для использования в повседневной медицинской практике.
Современные окклюдеры обладают необходимыми качествами для использования:
- имеют легкую и удобную систему доставки непосредственно к дефекту,
- полностью выполняют отверстие дефекта,
- обладают способностью к репозиционированию и извлечению в сложных анатомических случаях.
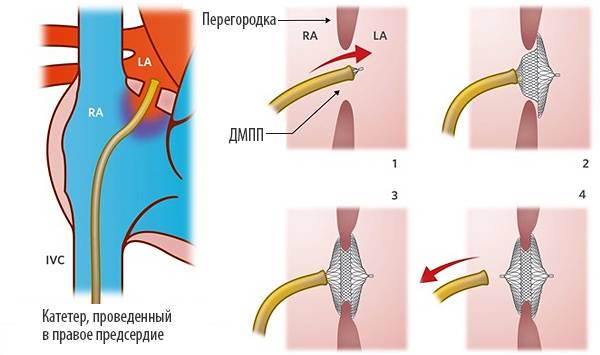 Этапы эндоваскулярной имплантации окклюдера ДМПП
Этапы эндоваскулярной имплантации окклюдера ДМПП
В мировой медицинской практике эндоваскулярное закрытие ДМПП стало операцией выбора, то есть первоочерёдным и оптимальным методом лечения. Закрытие вторичного ДМПП с помощью эндоваскулярной технологии с использованием окклюдера возможно в 80% случаев. Возможность эндоваскулярного метода лечения определяется анатомо-морфологическими характеристиками дефекта.
Преимущества методики:
- отсутствие разрезов и швов на теле;
- проведение операции через прокол бедренной вены;
- без наркоза, под местным обезболиванием;
- отсутствие длительной реабилитации после проведения операции;
- возможность вернуться к повседневной жизни через несколько дней после операции.
Для определения возможности выполнения операции эндоваскулярного закрытия ДМПП проводится трансторакальное Эхо-Кг и чреспищеводное Эхо-Кг.
После оценки показателей данных исследований принимается решение об анатомической и морфологичсекой возможности выполнения операции.
Дефект межжелудочковой перегородки у детей: диагностика и лечение в Израиле в национальном центре детской кардиохирургии.
Диагностика сердечно-сосудистых заболеваний и хирургическое лечение врождённых пороков сердца (ВПС) у детей — не единственная, но основная специализация врачей-экспертов из Центра детской кардиологии и кардиохирургии на базе МЦ «Хадасса».
Дефект межжелудочковой перегородки (ДМЖП) у плода, новорожденного или ребенка до 3 лет — с таким диагнозом впору впасть в панику: что теперь делать? помогут ли врачи? как избежать необратимых последствий? Однако, вместо того, чтобы отчаиваться, лучше попытаться понять природу заболевания, собрать информацию о диагностических и терапевтических методах, о врачах-специалистах. Проф. Эльдад Эрез, глава секции детской кардиохирургии в МЦ «Хадасса», врач-эксперт с богатым опытом в устранении дефекта межжелудочковой перегородки у детей считает, что это поможет найти оптимальное решение существующей медицинской проблемы. Что вы найдете в материале о ДМЖП сердца у детей, подготовленным проф. Эрезом?
- Клиническую характеристику дефекта межжелудочковой перегородки у новорождённого и ДМЖП сердца у детей
- Описание наиболее распространенных видов этого дефекта
- Информацию о диагностических процедурах и методах лечения ДМЖП, которые лучше всего подходят для детей и применяются в МЦ «Хадасса» (Израиль)
При малых ВПС ДМЖП признаки, свидетельствующие по результатам электрокардиографического исследования о перегрузке левого желудочка могут быть умеренными или вовсе не выявляться. С помощью УЗИ можно определить интенсивность потока крови через отверстие. Уточнение диагноза возможно после проведения катетеризации сердца или ангиографического исследования. Вводимое в левый желудочек рентгенконтрастное вещество, демонстрирует на ангиокардиограмме сброс крови сквозь незначительный по размерам перимембранозный дефект. Что же касается больших дефектов межжелудочковой перегородки, то здесь по результатам ЭКГ устанавливается комбинированная гипертрофия всех камер сердца (желудочков и предсердий). Уточнение степени выраженности и характера ДМЖП возможно с помощью эхо- или ангиокардиографии.
Наши консультанты будут рады ответить на любой Ваш вопрос по поводу лечения врожденных пороков сердца у детей в Израиле. Заполните форму, Вам перезвонят в самое ближайшее время.
9.6. ОТКРЫТЫЙ АРТЕРИАЛЬНЫЙ ПРОТОК
Открытый артериальный проток – порок, характеризующийся незаращением сосуда между лёгочной артерией и аортой (боталлов проток) в течение 8 нед после рождения; проток функционирует во внутриутробном периоде, но его незаращение приводит к нарушениям гемодинамики.
Распространённость
Открытый артериальный проток наблюдают в общей популяции с частотой 0,3%. Он составляет 10-18% всех врождённых пороков сердца.
ГЕМОДИНАМИКА
Наиболее часто артериальный проток соединяет лёгочную артерию и нисходящую аорту ниже отхождения левой подключичной артерии, реже он соединяет лёгочную артерию и нисходящую аорту выше отхождения левой подключичной артерии (рис. 9-5). Через 2-3 дня (реже через 8 нед) после рождения проток закрывается. У недоношенных детей, при гипоксии плода, перенесённой фетальной краснухе (в I триместре беременности) проток остаётся открытым. Возникает сброс (шунтирование) крови из нисходящей аорты в ствол лёгочной артерии. Дальнейшие проявления порока зависят от диаметра и длины открытого артериального протока и сопротивления кровотоку в самом протоке.
 Рис. 9-5. Анатомия и гемодинамика при открытом артериальном протоке. А – аорта; ЛА – лёгочная артерия; ЛП – левое предсердие; ЛЖ – левый желудочек; ПП – правое предсердие; ПЖ – правый желудочек; НПВ – нижняя полая вена; ВПВ – верхняя полая вена. Сплошная часть стрелки обозначает патологический поток крови из аорты в лёгочные артерии.
Рис. 9-5. Анатомия и гемодинамика при открытом артериальном протоке. А – аорта; ЛА – лёгочная артерия; ЛП – левое предсердие; ЛЖ – левый желудочек; ПП – правое предсердие; ПЖ – правый желудочек; НПВ – нижняя полая вена; ВПВ – верхняя полая вена. Сплошная часть стрелки обозначает патологический поток крови из аорты в лёгочные артерии.
• При малом размере протока и высоком сопротивлении шунта объём сбрасываемой крови незначителен. Поступление избыточного количества крови в лёгочную артерию, левое предсердие и левый желудочек также мало. Направление сброса крови в течение систолы и диастолы остается постоянным (непрерывным) – слева (из аорты) направо (в лёгочную артерию).
• При большом диаметре протока в лёгочную артерию будет поступать значительное избыточное количество крови, приводя к повышению давления в ней (лёгочной гипертензии) и перегружая левое предсердие и левый желудочек объёмом (следствием этого являются дилатация и гипертрофия левого желудочка). Со временем развиваются необратимые изменения в лёгочных сосудах (синдром Айзенменгера) и сердечная недостаточность. В дальнейшем давление в аорте и лёгочной артерии уравнивается, а затем в лёгочной артерии становится выше, чем в аорте. Это приводит к изменению направления сброса крови – справа (из лёгочной артерии) налево (в аорту). Впоследствии возникает правожелудочковая недостаточность.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Проявления порока зависят от размеров открытого артериального протока. Открытый артериальный проток с небольшим сбросом крови может не манифестировать в детском возрасте и проявиться с возрастом быстрой утомляемостью и одышкой при физической нагрузке. При большом объёме сбрасываемой крови с детства имеются жалобы на одышку при физической нагрузке, признаки ортопноэ, сердечной астмы, боли в правом подреберье вследствие увеличения печени, отёки ног, цианоз ног (в результате сброса крови справа налево в нисходящую аорту), цианоз левой руки (при открытом артериальном протоке выше отхождения левой подключичной артерии).
При малом объёме сброса крови слева направо внешних признаков порока нет. При сбросе крови справа налево появляется цианоз ног, изменения пальцев ног в виде “барабанных палочек”, изменения пальцев левой руки в виде “барабанных палочек”.
Пальпация
При интенсивном сбросе крови слева направо определяется систолическое дрожание грудной клетки над лёгочной артерией и супрастернально (в яремной ямке).
Аускультация сердца
9.2. ТЕТРАДА ФАЛЛО
Тетрада Фалло – врождённый порок сердца, характеризующийся наличием четырёх компонентов: 1) большого высокорасположенного ДМЖП; 2) стеноза лёгочной артерии; 3) декстропозиции аорты; 4) компенсаторной гипертрофии правого желудочка.
Распространённость
Тетрада Фалло составляет 12-14% всех врождённых пороков сердца.
ГЕМОДИНАМИКА
При тетраде Фалло аорта располагается над большим ДМЖП и над обоими желудочками, в связи с чем систолическое давление в правом и левом желудочках одинаковое (рис. 9-2). Главный гемодинамический фактор – отношение между сопротивлением кровотоку в аорте и в стенозированной лёгочной артерии.
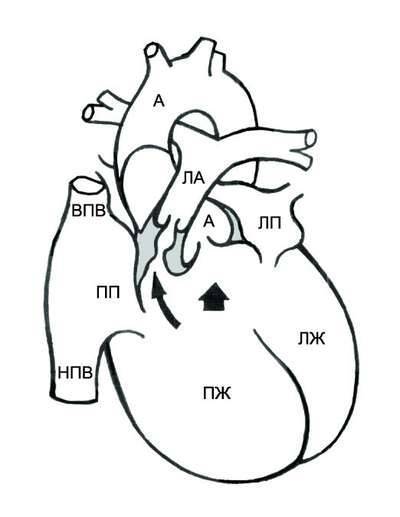 Рис. 9-2. Анатомия и гемодинамика при тетраде Фалло. А – аорта; ЛА – лёгочная артерия; ЛП – левое предсердие; ЛЖ – левый желудочек; ПП – правое предсердие; ПЖ – правый желудочек; НПВ – нижняя полая вена; ВПВ – верхняя полая вена. Короткая стрелка указывает на дефект межжелудочковой перегородки, длинная – на подклапанный стеноз лёгочной артерии.
Рис. 9-2. Анатомия и гемодинамика при тетраде Фалло. А – аорта; ЛА – лёгочная артерия; ЛП – левое предсердие; ЛЖ – левый желудочек; ПП – правое предсердие; ПЖ – правый желудочек; НПВ – нижняя полая вена; ВПВ – верхняя полая вена. Короткая стрелка указывает на дефект межжелудочковой перегородки, длинная – на подклапанный стеноз лёгочной артерии.
• При небольшом сопротивлении в лёгочных сосудах лёгочный кровоток может быть вдвое больше кровотока в большом круге кровообращения, и насыщение артериальной крови кислородом может быть нормальным (ацианотичная тетрада Фалло).
• При значительном сопротивлении лёгочному кровотоку возникает сброс крови справа налево, в результате чего возникают цианоз и полицитемия.
Стеноз лёгочной артерии может быть инфундибулярным или комбинированным, реже клапанным (подробнее об этом см. в главе 8 “Приобретённые пороки сердца”).
При физической нагрузке происходит увеличение притока крови к сердцу, но кровоток через малый круг кровообращения не возрастает из-за стенозированной лёгочной артерии, и избыточное количество крови сбрасывается в аорту через ДМЖП, поэтому цианоз усиливается. Возникает гипертрофия, что приводит к усилению цианоза. Гипертрофия правого желудочка развивается вследствие постоянного преодоления препятствия в виде стеноза лёгочной артерии. В результате гипоксии развивается компенсаторная полицитемия – увеличивается количество эритроцитов и гемоглобина. Развиваются анастомозы между бронхиальными артериями и ветвями лёгочной артерии. У 25% больных обнаруживают правостороннее расположение дуги аорты и нисходящей аорты.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Основной жалобой взрослых больных тетрадой Фалло является одышка. Кроме того, могут беспокоить боли в сердце без связи с физической нагрузкой, сердцебиение. Больные склонны к лёгочным инфекциям (бронхиты и пневмонии).
Осмотр
Отмечают цианоз, степень выраженности которого может быть различной. Иногда цианоз настолько выражен, что синеют не только кожные покровы и губы, но также слизистая оболочка полости рта, конъюнктива. Характерно отставание в физическом развитии, изменение пальцев (“барабанные палочки”), ногтей (“часовые стёкла”).
Пальпация
Обнаруживают систолическое дрожание во II межреберье слева от грудины над участком стеноза лёгочной артерии.
Аускультация сердца
Выслушивают грубый систолический шум стеноза лёгочной артерии во II-III межреберьях слева от грудины. II тон над лёгочной артерией ослаблен.
Лабораторные исследования
Общий анализ крови: высокий эритроцитоз, повышение содержания гемоглобина, СОЭ резко снижена (до 0-2 мм/ч).
Электрокардиография
Электрическая ось сердца обычно смещена вправо (угол α от +90° до +210°), отмечают признаки гипертрофии правого желудочка.
Эхокардиография
ЭхоКГ позволяет обнаружить анатомические составляющие тетрады Фалло.
Рентгенологическое исследование
Отмечают повышенную прозрачность лёгочных полей из-за уменьшения кровенаполнения лёгких. Контуры сердца имеют специфическую форму “деревянного башмака сабо”: уменьшенная дуга лёгочной артерии, подчёркнутая “талия сердца”, закруглённая и приподнятая над диафрагмой верхушка сердца. Дуга аорты может быть справа.
ОСЛОЖНЕНИЯ
Наиболее часто возникают инсульты, ТЭЛА, выраженная сердечная недостаточность, инфекционный эндокардит, абсцессы мозга, разнообразные аритмии.
ЛЕЧЕНИЕ
Единственный метод лечения – хирургический (радикальная операция – пластика дефекта, устранение стеноза лёгочной артерии и смещение аорты). Иногда хирургическое лечение состоит из двух этапов (первым этапом ликвидируют стеноз лёгочной артерии, а вторым проводят пластику ДМЖП).
Прогноз
 Пациенты с дефектами в перегородке длительно живут при соблюдении рекомендаций, которые указаны лечащим врачом. Прогноз при незначительном диаметре отверстия в ней благоприятный. Установление диагноза дает возможность раннего проведения операции и возвращения ребенка к нормальному ритму жизни.
Пациенты с дефектами в перегородке длительно живут при соблюдении рекомендаций, которые указаны лечащим врачом. Прогноз при незначительном диаметре отверстия в ней благоприятный. Установление диагноза дает возможность раннего проведения операции и возвращения ребенка к нормальному ритму жизни.
После проведения реконструктивной процедуры 1% людей доживает только до 45 лет. Больные старше 40 лет (около 5% от общего числа в указанной возрастной группе), которые были прооперированы по причине сердечного порока, погибают от осложнений, связанных с хирургическим вмешательством. Независимо от вероятности их присоединения, около 25% больных умирает при отсутствии помощи.
При наличии недостаточности кровообращения 2 стадии и выше, пациента направляют на медико-социальную экспертизу (МСЭ). Инвалидность устанавливается на 1 год после операции. Такая процедура проводится для нормализации гемодинамики. Ее одобряют не только при наличии хирургического вмешательства, но и в сочетании с недостаточностью кровообращения.
Родители должны помнить, что своевременная операция вернет ребенка в обычный ритм жизни. Лечение детей с пороками – это одно из приоритетных направлений в медицине. Наличие социальных квот, предоставляемых государством, позволяет бесплатно сделать операцию ребенку.
Диагностические методы
Методы диагностики ДМЖП:
- Сбор анамнеза. Опрос родителей насчет наследственных заболеваний, наличие сердечных патологий у родственников, течение беременности, принимаемые в первом триместре препараты и перенесенные болезни и т. д.
- Врачебный осмотр. Состоит из измерения пульса, аускультации сердца (прослушивания шумов), осмотра цвета кожных покровов и изменения формы грудной клетки, пальпации в области сердца. При ДМЖП этот метод в большинстве случаев уже позволяет поставить диагноз.
- Эхокардиография. Дефект отображается в виде разрыва эхосигнала в межжелудочковой перегородке со сбросом, выявленным в режиме непрерывно-волнового и цветного допплера.
- МРТ. Проводится при недостаточности сведений ЭхоКГ или смазанности результата.
- Катетеризация сердечных полостей. Позволяет проверить гемодинамику малого круга кровообращения, количество, размер и размещение дефектов, наличие сопутствующих аномалий.
- Рентгенография. Применяется для диагностики больших ДМЖП и легочной гипертензии. Малые дефекты не отображаются.
- ЭКГ. Диагностируются как малые, так и крупные дефекты по отклонению оси.
- Лабораторная диагностика. Общий анализ крови берется для определения уровня гемоглобина. Делается при необходимости хирургического вмешательства.
Прогнозы на выздоровление
Говорить о благополучном исходе операции и лечения в целом можно только, опираясь на данные о своевременном назначении терапии
Важно, чтобы до операции не возникло никаких осложнений. 95% малышей, рожденных с патологией перегородки, живут и развиваются, как и все здоровые дети
Смертность при ДМПП – явление редкое. Без лечения люди могут дожить до 40 лет, а далее прогнозируется инвалидность. При устранении дефекта в младенчестве человек может рассчитывать на полноценную жизнь. Иногда отмечается возникновение аритмии в возрасте 20-25 лет.
Диагностика сердечных патологий
Дефект перегородки можно обнаружить и в процессе планового медосмотра. Как правило, первые подозрения на ДМПП возникают после проведения аускультации (слышны шумы в сердце). Дает возможность обнаружить патологию и УЗИ сердца (эхокардиограмма).

ДМПП на ЭхоКГ
Если ваш лечащий врач подозревает вышеуказанное отклонение в функционировании сердца, чтобы подтвердить диагноз понадобятся специфические методы исследования:
- уже указанная выше эхокардиограмма (оценивает работу сердечной мышцы и ее состояние);
- рентгенография грудной клетки (дает возможность обнаружить расширение отдельных отделов. Если на снимке видно расширение правых отделов, скорее всего, у пациента присутствует патология ДМПП);
- пульсоксиметрия (метод изучения крови на предмет содержания кислорода. Процедура абсолютно безболезненна для ребенка, выполняется с помощью датчика, он и подсчитывает количество кислорода);
- катетеризация сердца (через артерию с помощью катетера в систему кровотока впрыскивается контрастное вещество, с помощью снимков фиксируется его путь. Это позволяет сделать выводы о функциональном состоянии сердца и выявить патологию);
- МРТ(магнитно-резонансная томография) дает возможность оценить состояние структурных элементов сердца, не подвергая ребенка рентгеновскому излучению. Обычно, МРТ используют как дополнительный метод постановления диагноза, если результаты предыдущих исследований не дали однозначного ответа о наличии патологии.

ДМПП выявление

Клиника ДМПП
Анатомия порока
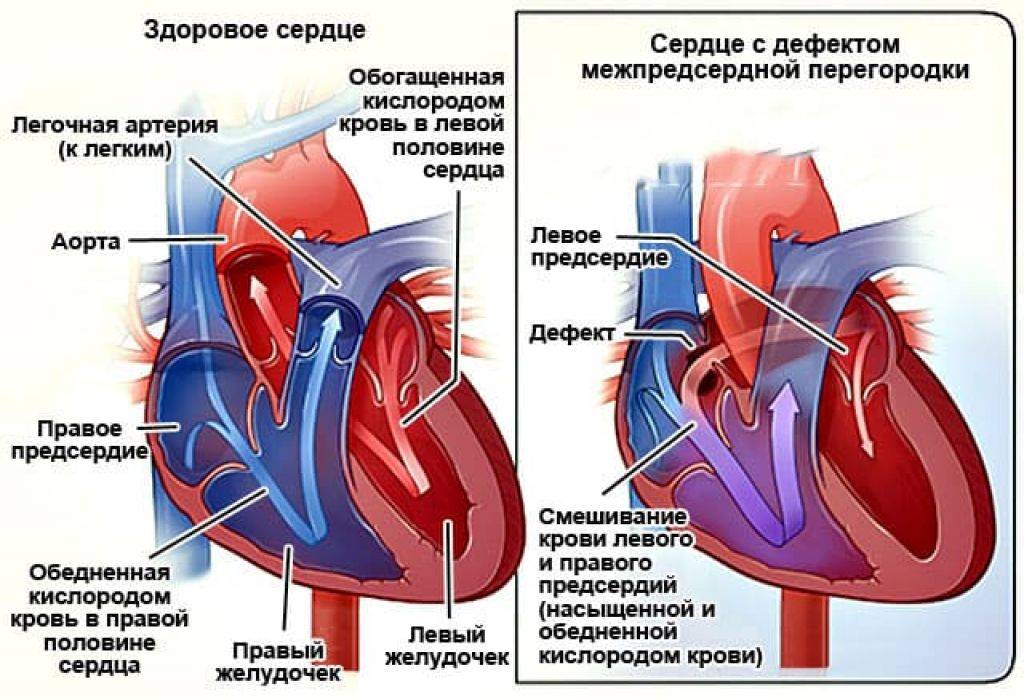
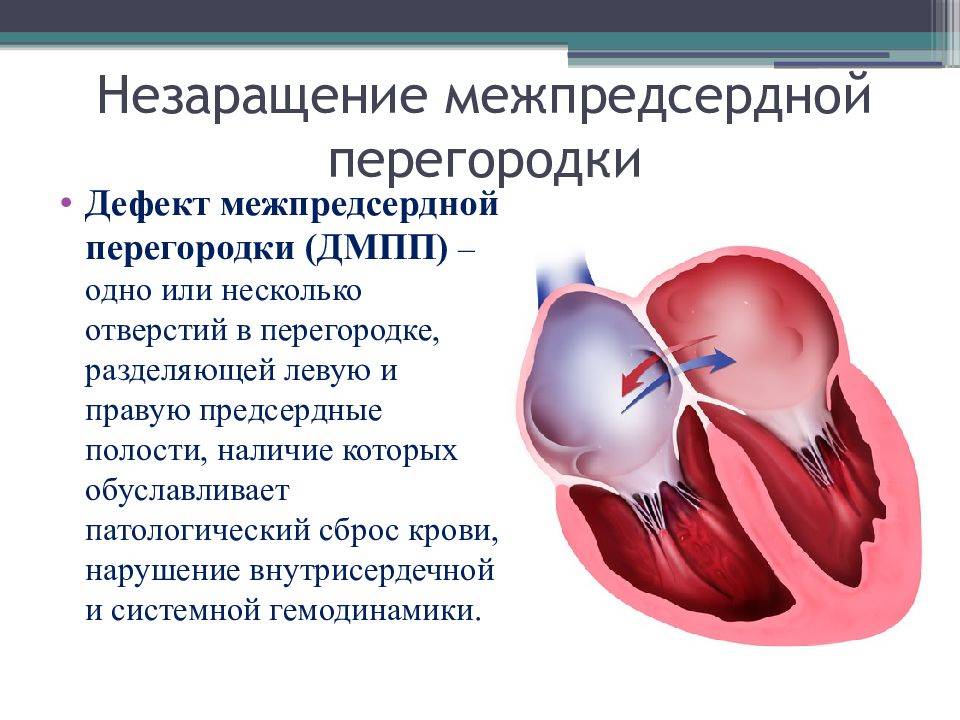
В здоровом сердце взрослого человека предсердия полностью изолированы друг от друга. Левое принимает кровь из легких, обогащенную кислородом и готовую к доставке ко всем органам. В правом предсердии находится венозная кровь с очень небольшим содержанием кислорода. При ВПС ДМПП, когда между предсердиями есть патологическое отверстие, происходит перемещение крови из левого предсердия в правое.
Чем грозит подобная аномалия? Правая часть сердца отвечает за перекачку крови в легкие, чтобы она насытилась кислородом. При забросе дополнительного количества крови происходит перегрузка легочных сосудов. Лишний объем крови может вызывать сердечную недостаточность и рост давления в легочной артерии (легочную гипертензию).